ADE效应是导致登革出血热和登革休克综合症的主要方式,后果很可能致命
登革病毒主要引起的登革热(dengue fever,DF)并非一种很恐怖的疾病,大部分人可能发发烧,关节痛,过几天就好了,但是对于登革病毒来说,恐怖的是二次感染,这种感染会因为第一次感染后机体产生的非中和性的抗体可以促进非同一血清型病毒感染,进而加重病情(也就是抗体依赖的增强作用,antibody-dependent enhancement,ADE),这是导致登革出血热(dengue hemorrhagic fever,DHF)和登革休克综合征(dengue shock syndrome,DSS)的主要方式,而后两种疾病则很可能是致命的。所以建议广东大爆发时候的登革患者少去东南亚旅行,如果去旅行的话也一定做好防蚊措施。
今天介绍的是洛克菲勒大学团队在《Science》上的有意思的发现——IgG antibodies to dengue enhanced for FcγRIIIA binding determine disease severity。
摘要:Dengue virus (DENV) infection in the presence of reactive, non-neutralizing immunoglobulin G (IgG) (RNNIg) is the greatest risk factor for dengue hemorrhagic fever (DHF) or dengue shock syndrome (DSS). Progression to DHF/DSS is attributed to antibody-dependent enhancement (ADE); however, because only a fraction of infections occurring in the presence of RNNIg advance to DHF/DSS, the presence of RNNIg alone cannot account for disease severity. We discovered that DHF/DSS patients respond to infection by producing IgGs with enhanced affinity for the activating Fc receptor FcγRIIIA due to afucosylated Fc glycans and IgG1 subclass. RNNIg enriched for afucosylated IgG1 triggered platelet reduction in vivo and was a significant risk factor for thrombocytopenia. Thus, therapeutics and vaccines restricting production of afucosylated, IgG1 RNNIg during infection may prevent ADE of DENV disease.
摘要已经简明扼要的把这篇研究的重点内容点出来了——DHF/DSS是由非中和性IgG抗体(RNNIg)介导的ADE效应,但是DHF/DSS发生的群体中并不是所有患者都有RNNIg存在,所以单独RNNIg本身并不能决定疾病的严重性,从这一点出发,作者发现DHF/DSS患者产生的IgG1亚类抗体对于非岩藻糖化的Fc受体FcγRIIIA 具有很高的亲和力(可以理解为结合在一起不分开),而这两者的结合诱导了血小板的减少,这也是血小板减少综合征的一个重要的危险因素,所以针对非岩藻糖化的IgG1 RNNIg的疫苗或者治疗方法可能防止登革病毒的ADE效应。
————————————
在这篇文章出来之前,学术界对登革病毒ADE效应的原因有以下解释:非中和性抗体可以促进病毒感染表达γFc受体的细胞。免疫复合物(抗原抗体结合在一起的东西)可以介导病毒进入并感染更多的细胞,还可以促进细胞之间的融合,并且可以抑制固有免疫应答。
抗体首先是一个Y型结构,两条轻链两条重链组成,重链的后两段或三段恒定区就是Fc段,这一段在多种细胞上有受体,通称Fc段受体(FcR),但是大多数Fc和FcR结合的亲和力一般比较弱,所以一般情况下,很多抗原-抗体聚集在一起形成免疫复合物,这样很多Fc段聚集在一起,进而可以结合很多个FcR,这样才能牢牢的相互作用并激活下游信号。比如吞噬细胞上的FcR可以通过结合已经抓住抗原(免疫复合物)的抗体Fc段来吞噬抗原,这就是抗体的调理作用(opsonization)。还有ADCC效应,也就是抗体依赖的细胞介导的细胞毒作用(antibody-dependent cellular cytotoxicity ),这是病毒感染的细胞会把病毒抗原展示在细胞表面,抗体结合上去之后,NK细胞等杀伤细胞通过FcR结合这些细胞,进而把这些细胞裂解掉。但是FcR也有抑制炎性免疫应答的功能。
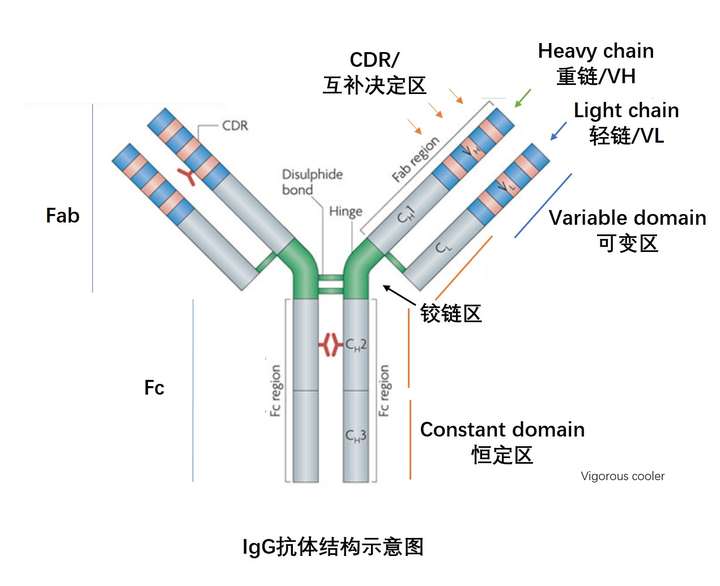
FcR介导的是激活信号还是抑制作用主要由Fc的结构决定,而Fc的结构又由IgG的亚类和CH2结构域上N连接的糖基化位置所决定。
人体中存在五类抗体,分类的依据是重链抗原性的差异,总共五种:μ链、γ链、α链、δ链和ε链,对应的分别是IgM、IgG、IgA、IgD和IgE。
人IgG可分为四个亚类——IgG1、IgG2、IgG3和IgG4。血清里IgG1和IgG2含量最高,两者在抗原特异性IgG中占比95%。不同亚类的抗体结合抑制型和激活型的FcR有不同的比例。Fc段CH2上天冬酰胺(Asn/N)上有核心的七糖结构(下图上部除中间最下外的浅蓝色部分),这个结构可以添加不同的糖来修饰。没有岩藻糖修饰的聚糖对于FcγRIIIA 亲和力更强,而岩藻糖和唾液酸化糖链的IgG更倾向于结合FcγRII。
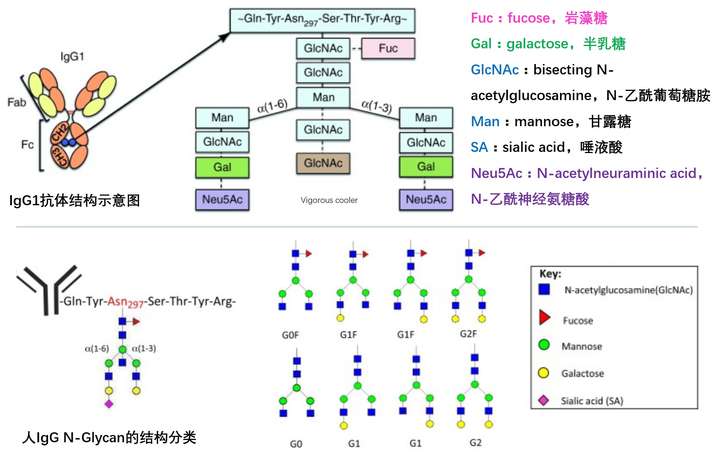
【注】:抗体的糖基化修饰种类很多,主要的是N-Glycan,N-Glycan根据半乳糖基化的数量可以分G0(无半乳糖)、G1(一个半乳糖基)和G2(两个)三类,再根据唾液酸化的数量可以命名为G2A0、G2A1等等,再根据有无分叉(bisecting)的N-乙酰葡萄糖胺(B)和岩藻糖(F)可以+B+F或者+B-F等等;除了N-Glycan外还有七糖不完整的类型;除了N-Glycan外还有甘露糖(Mannose)型的。
————————————
作者据此推测很可能IgG的不同Fc段对于登革病毒的ADE可能有一定的决定作用,所以他们对住院的二次登革患者或者先前有其他黄病毒感染的登革患者进行了队列研究。并且规定了几个定义:这些病人在发病早期产生的抗体定义为RNNIg,而且所有患者都被诊断为DHF/DSS或者DF,采集的血样为急性期(发热4~8d)和恢复期(出院>30d),对照为诊断为流感病毒HA抗体阳性的流感患者(健康成人鼻腔感染H1N1野毒株,血样在感染前和感染后7d采集)。
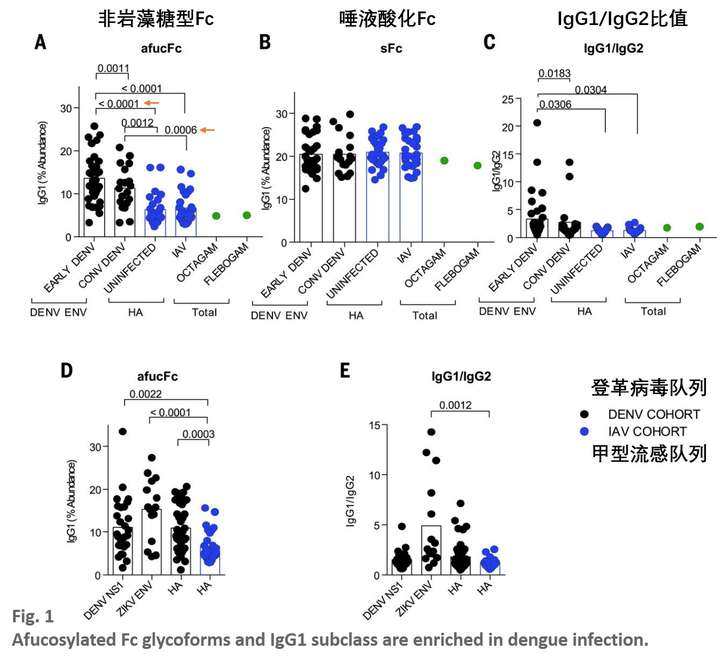
首先,相比IAV感染者,DENV感染的RNNIg+病人血清有大量的针对DENV E蛋白的非岩藻糖型IgG的升高(Fig.1A)(octagam和flebogam是两种成分为免疫球蛋白的药品),并且在急性期和恢复期针对E蛋白的IgG水平都比较高。但是唾液酸化的IgG没有区别(Fig.1B)。这些IgG更多倾向于IgG1型而非IgG2型(Fig.1C)。而这两个特点(IgG1型和非岩藻糖基化)都增强了抗体Fc段结合受体FcγRIIIA。
那么,产生的这些针对E蛋白的 afucFc型抗体 是不是仅局限于针对E蛋白呢?作者又试了NS1蛋白和寨卡病毒的E蛋白(交叉反应),发现这些抗体的 afucFc修饰水平也是上升的(Fig.1D)。从这些结果可以很好推断在登革病毒感染早期,IgG Fc的结构发生了整体性的较大转变。而且在产生的针对不同血清型E蛋白的afucFc抗体水平是大致相同的。针对寨卡病毒的E蛋白,IgG1/IgG2比值也是升高的,但是针对DENV NS1的却没有(Fig.1E),可能表明Fc段的岩藻糖化是登革感染过程中更普遍的特征。
————————————
分析了登革病人IgG抗体偏向afucFc之后,再区分一下登革热/DF和登革出血热/DHF或者登革休克综合症/DSS患者的抗体类型,结果发现DHF患者要明显比DF患者afucFc的水平高,也就说明重症登革患者中IgG1更倾向于afucFc修饰(Fig.2A)。而把血小板减少症的再单独抽出来,发现TH+的抗体倾向于afucFc修饰,而TH-的则与对照组没有差别(Fig.2B)。并且 afucFc大于10%则视为危险因素(P = 0.0139; 优势比 11.00; 95%置信区间1.635 to 74.00; 相对危险度1.833)。
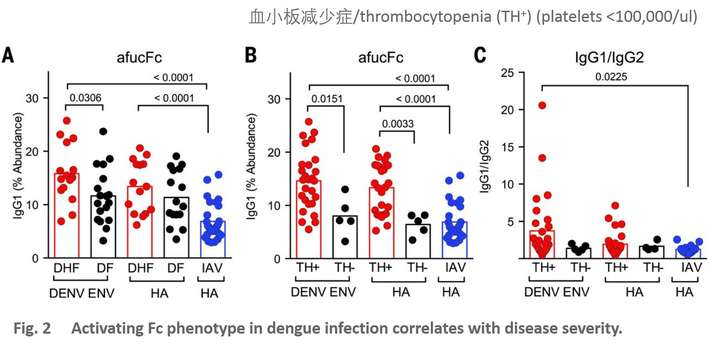
afucFc修饰除了和血小板减少症相关之外,还跟患者住院期间最低血小板计数相关(Fig.2D&E)。这两个危险因素跟抗体对FcγRIIIA的高亲和力也相关,患者如果有高水平的afucFc IgG1就很可能有严重的血小板减少症(Fig.2F), 队列中唯一进展为DSS的患者的afucFc IgG1水平是最高的(Fig.2F里加*号的)。
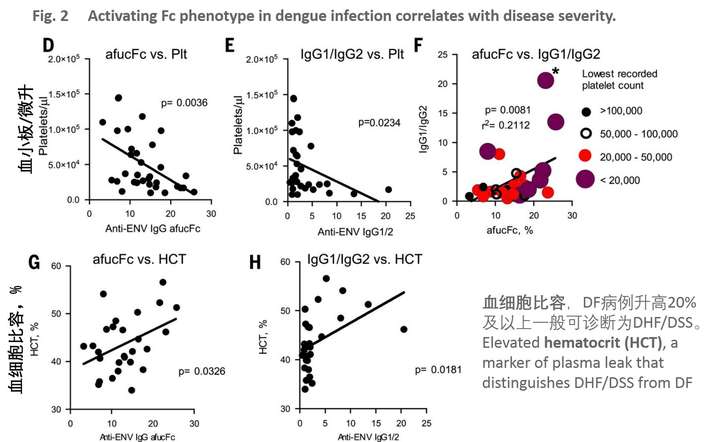
临床诊断DHF和DSS,除了看血小板减少外,还有一条是看血细胞比容/HCT,这也是血浆渗漏的一个标志。HCT也跟afucFc IgG1和针对E蛋白的IgG1/IgG2比值相关(Fig.2G&H)。

从上面这些结果,afucFc IgG1和疾病严重程度的相关性可能跟DENV感染过程中的ADE相关。而且,又跟血小板减少的关系那么密切,作者据此推测抗DENV的IgG很可能跟血小板的抗原相互反应,进而介导了DENV病程中血小板的减少,从而导致登革疾病中的ADE。
————————————
前期已有研究表明NS1抗体可以和血小板交叉反应,所以作者想是不是可以把TH+患者的血清中的IgG拿出来,转到其他个体中,是不是可以减少该个体的血小板?利用一个Fc受体人源化的小鼠模型,将TH+患者的IgG转进去之后,发现小鼠的血小板计数有明显的下降,而TH-患者的 IgG却对血小板计数没有影响(Fig.S3)。而把TH+患者的IgG处理去掉Fc段的聚糖之后 (TH+agly) (也就不能结合Fc受体了)几乎不能影响血小板的计数了。此外,所有FcRs都缺陷的小鼠则能抵抗TH+ IgG介导的血小板减少(Fig.3A)。而这种减少,依赖于两种人低亲和力Fc受体——FcγRIIA (CD32A) 和FcγRIIIA (CD16A),因为只缺失一种并不能介导小鼠对TH+患者的IgG介导的血小板减少的抵抗。
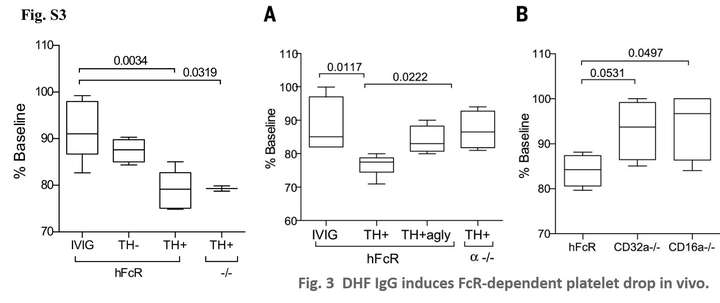
既然纯化的IgG可以介导血小板的减少,那么是不是TH+患者的IgG可以直接结合血小板?将IgG直接和小鼠或者人的血小板进行孵育,结果发现,从结合血小板上洗脱下来的抗体只能结合NS1而非E蛋白(Fig.S4&Fig.3C)。但是也是afucFc为主的(Fig.3D),但是IgG1/IgG2比值几乎没有变化(Fig.S5)。
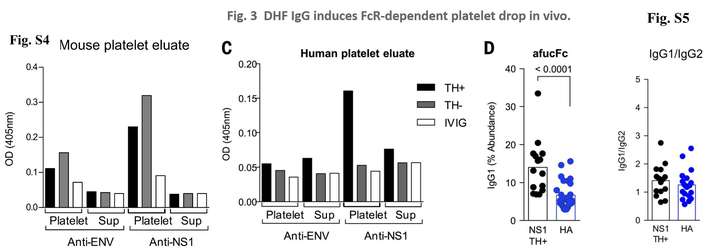
所以,综合下来,DENV感染过程中患者IgG对FcγRIIIA 亲和力升高,通过FcR依赖的血小板减少而导致了血小板减少症。而至少有三种机制促进了血小板的减少:[1] 抗NS1/IgG抗体可能通过血小板的FcγRIIA直接激活血小板;[2] 并/或者介导了单核细胞吞噬表达 FcγRIIIA和FcγRIIA的血小板;[3] 和/或FcγRIIIA介导的针对血小板的ADCC效应。
————————————
ADE的传统解释是抗体依赖的病毒感染增强作用,是结合非中和性抗体的病毒颗粒更容易进入原本进入不了的细胞,进而增强感染。本文的实验是证实针对登革病毒的IgG因为具有对FcγRIIIA 的高亲和力,进而导致了疾病的ADE效应。利用TH+和TH-的病人血清利用经典的U937实验都可以促进DENV的感染,但是并不能解释本文作者观察到的RNNIg+ DENV 患者的IgG可以激活FcRIIIA,因为U937细胞本身是 FcγRIIIA阴性, FcγRIIA阳性的(FcγRIIIA–, FcγRIIA+)(Fig.S6)。所以,本项研究把ADE的感染和ADE的疾病严重程度分开了。
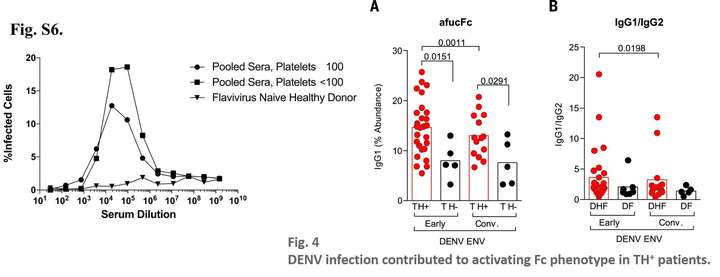
这种特殊的Fc结构到底是原本就存在还是由登革病毒感染所诱导的?作者比较了TH+患者在急性期和恢复期抗体Fc的水平,结果发现恢复期的抗体中 afucFc 型IgG和 IgG1/IgG2比值都明显的下降了(Fig. 4A&B),所以,应该是DENV的感染介导了FcγRIIIA高亲和性IgG的生成。
————————————
The present finding that some individuals respond to DENV infection by producing IgGs with higher affinity for FcγRIIIA indicates a host determinant of susceptibility to severe DENV disease. Further studies will determine how this patient selectivity may contribute to additional mechanisms underlying ADE of DENV disease.
总结:DENV感染诱导的FcγRIIIA高亲和性IgG是严重DENV疾病的一个危险因素。而进一步的研究将确定这种患者选择性如何可能有助于DENV疾病ADE的其他机制。比如那些基因的多态性等等。
完
原文连接:IgG antibodies to dengue enhanced for FcγRIIIA binding determine disease severity
参考资料:
[1] 人民卫生出版社第6版《医学免疫学》
[2] IMGT Lexique
[3] DOI: http://dx.doi.org/10.1016/j.pt.2011.08.003