他汀个体化用药基因检测
2019 年 8 月 31 日,万众瞩目的《2019 版血脂管理指南》在欧洲心脏病年会(ESC)上揭开面纱,其中最显而易见的变化是降脂目标的全面大幅下移,LDLc「低一些,好一点」,「挥别 1.8 时代,开启 1.4 时代」,成为新指南的亮点和关键点 [1]。尽管新指南继续稳固了他汀类药物在降低 LDLc 领域不可动摇的地位,面对这么大的降幅和这么低的 LDLc 目标值,如何个体化安全有效的应用他汀再度成为临床讨论的热点和面临的挑战。 他汀作为防治心血管疾病最广泛应用的降脂药,对大多数人而言,既安全,且耐受性良好;然而,他汀与肌肉毒性相关,其严重程度可从无肌酸激酶升高的轻度肌痛,到罕见并危及生命的自身免疫性坏死性肌炎的发生。
尽管随机对照试验(RCT)证明,他汀和安慰剂组之间不良事件发生率相似,但观察性研究显示,他汀药物相关肌肉症状(SAMS)的发生率高达 7% 至 29%。服用同等剂量的他汀,中国患者不良反应发生率还是欧洲患者的十倍,且程度更重。尽管轻度 SAMS 为自限性,但常常导致他汀药物的依从性差和停药,进而导致心血管事件和死亡率的增高 [2]。 由于药物疗效和副作用往往受遗传因素影响,致力于将基因遗传信息用于个体化药物治疗,以最大化发挥药物疗效,避免药物不良反应的药物基因组学研究是精准医学的重要组成部分。前期针对辛伐他汀肌病患者进行的全基因组关联性研究明确了 SAMS 的遗传因素源自溶质载体阴离子转运蛋白家族 1B1(SLCO1B1)基因的单核苷酸多态性 rs4149056(SLCO1B1* 5),该位点的 C 等位基因杂合子(CT)和纯合子(CC)携带者发生他汀肌病的风险分别是 TT 携带者的 4.5 倍和 17 倍 [3]。
由于 SLCO1B1*5 变异型导致所编码的肝脏有机阴离子转运多肽转运蛋白(OATP1B1)的活性降低,阻碍了辛伐他汀从血浆向肝脏的转运,故辛伐他汀的血浆浓度升高,肌病风险增加。由于 SLCO1B1* 5 等位基因携带者服用辛伐他汀的 SAMS 风险最大,而服用普伐他汀或瑞苏伐他汀的 SAMS 风险最小;因此,SLCO1B1*5 基因检测为个体化定制他汀治疗提供了机会。但是他汀药物治疗窗宽,除了辛伐他汀还有其他低成本他汀,而且临床常常难以对肌痛明确诊断;因此,在患者启动他汀治疗前进行药物基因检测具有很大的挑战性。2018 年,来自杜克大学精准医学中心的 Deepak Voora 教授团队在国际上首次发布了基因检测指导他汀个体化降脂治疗的 RCT 研究----GIST study,目的在于探索 SLCO1B1 基因检测是否能够改善有他汀肌病史的患者重启他汀治疗的依从性和疗效 [4]。
GIST 研究总计募集了 159 例明确有他汀肌病史的患者,将其随机分为 SLCO1B1 基因指导组(GIST 组,n = 83)和常规对照组 (n = 76)。所有入选患者重新启动他汀治疗,在 GIST 组中,SLCO1B1*5 携带者接受瑞舒伐他汀,普伐他汀或氟伐他汀治疗;非携带者服用既往未曾服用过的他汀进行治疗。在常规组中,所有患者接受既往未服用过的他汀进行治疗。主要终点事件是重启他汀治疗的依从性;次要终点事件包括:重启他汀的患者例数,低密度脂蛋白胆固醇(LDLc)水平,以及患者对他汀治疗的看法。通过倾向性评分,本研究还比较了 1907 例接受 SLCO1B1 基因检测患者和未检测基因的对照组患者之间 LDLc 水平的差异。 结果发现,本研究 25% 的受试者携带 SLCO1B1*5 等位基因,尽管他汀用药依从性在两组之间无明显差异,但是与常规治疗组相比,GIST 组的新他汀处方更多(55.4%vs.38.0%; P = 0.04)(图 1),治疗 3 个月时的 LDLc 水平更低(131.9±42.0 vs.144.4±43.0 mg/dL; P = 0.04)(图 2)。试验结束后,常规治疗组获知 SLCO1B1 检测结果并接受基因指导治疗的患者与 GIST 组的患者相比,LDLc 水平还有额外的降低(-14.9±37.8 vs. 9.0±37.3 mg/dL; P = 0.03)。在本研究后续 5 年随访的观察性研究中也证实,与相匹配未经基因检测的对照组患者相比,接受 SLCO1B1 基因检测的患者 LDLc 水平降低得更多 (−1.8±0.8 mg/dL /年, P = 0.04)(图 3)。除此之外,本研究还发现,GIST 组患者对他汀药物的认知较常规组有更好的改善趋势。
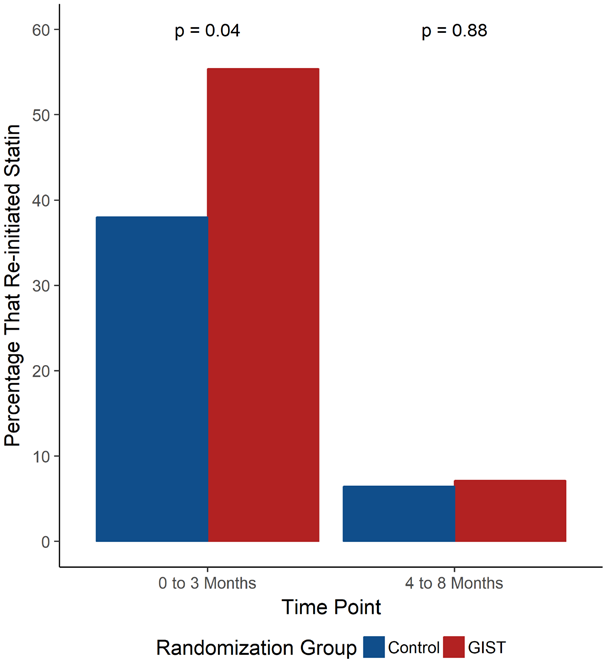
图 1. 重启他汀治疗的患者百分数。 GIST indicates Genotype Informed Statin Therapy,基因指导组;Control,常规治疗组.
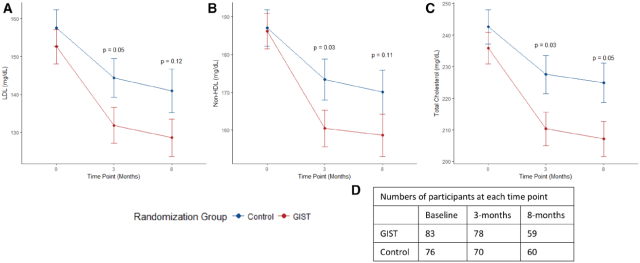
图 2. 基线以及随机 3 个月和 8 个月的平均胆固醇测量值。A) LDLc, B) non-HDLc; C) total cholesterol GIST indicates Genotype Informed Statin Therapy,基因指导组;Control,常规治疗组.
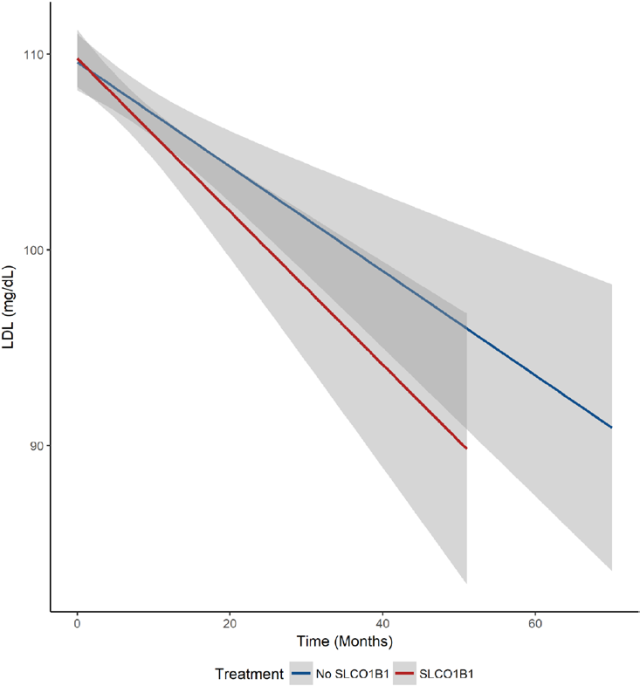
图 3:LDLc 随时间变化的线性回归分析。红色:接受 SLCO1B1 基因检测指导他汀治疗的患者,蓝色:1:1 倾向性评分匹配的未接受 SLCO1B1 基因检测指导他汀治疗的患者。
GIST 研究是国际上首个应用 SLCO1B1 基因检测指导他汀重启的前瞻性随机对照研究。尽管未能证实基因检测能够改善他汀用药的依从性,但该研究证实,基因检测能够帮助更多有肌病史的患者重启他汀治疗,并更有效的降低 LDLc 水平。虽然 SLCO1B1 基因分型增加了重启他汀治疗的患者人数,但试验中他汀重启的总体发生率(39%)仍低于前期预期值(60%),故降低了本研究观察主要终点事件----他汀药物依从性的能力。
尽管基因检测有助于增加重启他汀治疗的患者数,由于药物依从性受多因素影响,还需要其他干预手段提高患者他汀用药的依从性,例如:加强医务人员对患者的科普教育,增设对患者用药的数字化提醒服务等。 通过对预设的次要终点事件评估,GIST 研究还证实,SAMS 是降低心血管风险的重要障碍,进行 SLCO1B1 基因检测能够调动医生为患者重启他汀治疗的意愿,并改善患者对他汀治疗的认知。上述转变带来的是基因指导下,GIST 组患者 LDLc 水平降低 20 mg/dL;以及试验结束后,常规组患者接受基因指导治疗后的 LDLc 水平降低 14.9 mg/dL。
而且,与常规治疗组相比,SLCO1B1*5 携带者在 GIST 组中应用瑞舒伐他汀,普伐他汀或氟伐他汀降脂治疗的比例更高(92%vs.67%);接受基因检测后的 SLCO1B1 * 5 携带者的 LDLc 降幅更大。这表明,通过基因检测获得新的药物治疗方案能够帮助患者取得更好的药物疗效。 由于药物基因检测临床推广的障碍主要来自循证医学证据的缺乏,开展基因检测指导用药对临床转归和成本效益影响的 RCT 研究十分必要。严格设计的 RCT 是制定药物基因检测相关临床指南以及医保政策的重要前提,然而,由于研究成本高,以及高风险等位基因罕见现象的存在,难以对每个风险等位基因-药物对都提供强有力的 RCT 证据。
国际诸多医疗中心已开始对药物反应密切相关的基因型进行临床检测,美国国立卫生院资助的临床药物遗传学实施联盟(CPIC)已经发布了 30 种基因-药物对的临床应用指南,其中包括 SLCO1B1 与辛伐他汀,为药物基因检测转化为临床处方决策提供了重要的参考依据 [5]。尽管如此,即使是经过充分证实的药物相关基因位点,仍不能完全解释药物的所有个体差异。因此,药物基因检测并不是提高药物疗效的神奇法宝,而是帮助我们更接近个体化用药的重要手段之一。 总之,GIST 研究表明,SLCO1B1*5 基因检测指导他汀用药的重启能够带来临床获益且无危害。 在 ESC 发布的《2019 版血脂管理指南》坚持他汀在胆固醇管理中的首选地位,且强调「LDLc 越低越好」的理念和新的降脂目标的指导下,基因检测将为临床如何个体化安全有效的强化他汀治疗提供新的解决思路。
参考文献
1. 2019 ESC/EAS Guidelines for the management of dyslipidaemias: lipid modification to reduce cardiovascular risk: The Task Force for the management of dyslipidaemias of the European Society of Cardiology (ESC) and European Atherosclerosis Society (EAS) . European Heart Journal, ehz455 https://doi.org/10.1093/eurheartj/ehz455,Aug, 2019
2. Rasmussen JN, et al. Relationship between adherence to evidence-based pharmacotherapy and long-term mortality after acute myocardial infarction. JAMA. 2007;297:177–186. 3. Link E, et al. SLCO1B1 variants and statin-induced myopathy–a genomewide study. N Engl J Med. 2008;359:789–799.